
蛋白序列分析是指解析蛋白质分子的氨基酸序列,从而揭示蛋白质的结构。这一过程不仅仅是对蛋白质分子进行简单的结构描述,更是深入了解蛋白质功能、相互作用、疾病机制以及药物靶点的重要途径。蛋白质各种各样,每个蛋白质都有自己特定的三维结构,每个结构都有特定的功能。蛋白质的功能依赖于其结构,而结构由氨基酸序列决定。因此,理解和测定氨基酸序列对于研究蛋白质功能和表达至关重要。例如镰刀型细胞贫血病(因β-肽链第6位氨基酸谷氨酸被缬氨酸所代替,构成镰状血红蛋白,取代了正常血红蛋白)。蛋白序列分析可以帮助科研人员确定未知蛋白的氨基酸组成,识别蛋白质的翻译后修饰,并揭示其空间结构与功能之间的关系。例如,蛋白质的序列以及N/C端对蛋白合成和过表达都有重要的意义:(1)在蛋白质合成过程中,蛋白质的半衰期与多肽链N-端特异的氨基酸有关,它们对蛋白质的寿命有控制作用。并且N端可发生多种翻译后修饰(例如组蛋白的N端尾巴),这些也与蛋白质的功能和稳定性息息相关。(2)在蛋白表达时,可能会受到外肽酶影响,从而表达的蛋白N/C端会有部分氨基酸缺失。此外,蛋白序列分析在生物医药、疾病诊断、靶向治疗、抗体药物开发、疫苗设计等领域都有着广泛的应用。例如,在药物开发领域,蛋白序列的分析检测可用于验证重组蛋白药物的纯度和稳定性,确保药物的安全性和有效性;在疾病研究中,通过对异常表达或突变的蛋白进行序列分析,能够揭示疾病发生发展的分子机制,为精准医疗提供有力支持。
一、蛋白序列分析检测方法
1、Edman降解法
埃德曼降解法(Edman degradation method)是蛋白质或肽的氨基末端分析法之一,也是常规方法。通过Edman降解法分析N端的15个氨基酸序列在生物药申报时通常是必检项目;同时也是很多已上市生物药的年检项目。
Edman的大致流程为:在弱碱性条件下使之与异硫氰酸苯酯反应,然后用酸处理,从多肽链上仅使氨基末端残基以氨基酸的苯基乙内酰硫脲衍生物的形态游离出来,然后进行分析(常规是液相),剩余的肽段进行下一步循环反应。根据反应试剂或衍生物的缩写,本法亦称PTC法或PTH法。
利用Edman降解法一次能连续测出50-60个氨基酸序列,其优点是:①可以准确分析N端氨基酸序列,特别是能辨别异亮氨酸和亮氨酸、谷氨酰胺和赖氨酸;②灵敏度高;③可靠直接,和质谱法相比较不依赖于数据库。
当然,Edman降解法也有一定的局限性,例如:通量较低,一个循环只能测一个氨基酸;N端被修饰封闭时,无法直接测序,需要先除去这些基团,才能测序;不能直接测试含二硫键的半胱氨酸的序列等。
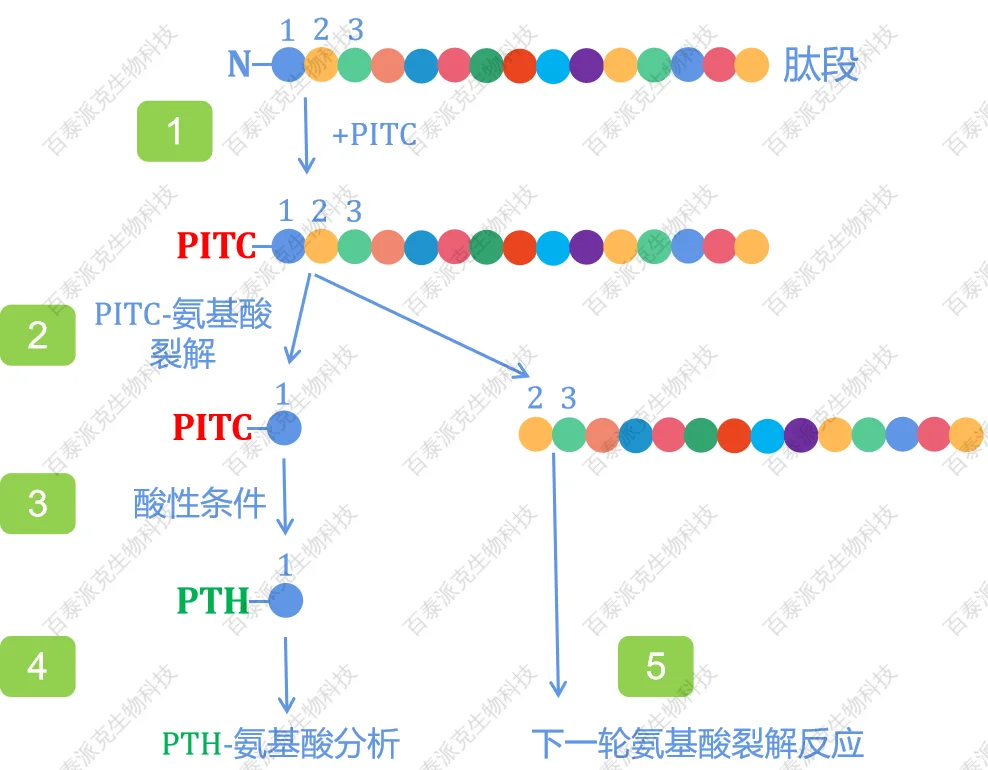
图1. Edman降解法流程
2、质谱法
除了Edman降解法,质谱技术(尤其是串联质谱)也被广泛用于蛋白质的氨基酸序列分析,具有高通量的特点。质谱法将蛋白酶切成长短不一的肽段(常规在5-30个氨基酸),随即通过LC-MS/MS分析检测,将采集的数据与理论序列数据库进行匹配,进而确认N端序列,质谱可以测出封闭和修饰的蛋白N末端。
一般来说,如果多肽链只断裂成两段或者三段便能测出它们的氨基酸序列,也就不难推断出在原来多肽中的前后次序,只要知道原多肽链的C端和N端的氨基酸即可,除非末端残基恰好与切口的氨基酸一样才不能得出结论。然而多数场合,断裂得到的肽段多于此数目,因此除了能确定N/C端的肽段位置外,中间那些肽段的次序还是不能肯定。为此,需要用两种或两种以上的不同方法断裂多肽样本,使其成两套或者几套的肽段。不同断裂的方法是指断裂的专一性不同(酶不同),即切口是彼此错位的,因为多套肽段可以互相跨过切口而重叠(overlap),这种跨过切口而重叠的肽段称为重叠肽(overlaping peptide)。
借助重叠肽可以确定肽段在原多肽链中的正确次序,拼凑出整个多肽链的氨基酸序列。同时,多套肽段可以互相核对各个肽段的氨基酸序列测定中是否有差错。此方法的过程即是氨基酸全序列重建的过程。如果有数据库参考,可验证蛋白与理论序列的一致性。在分离出一些新的蛋白,没有理论序列参考的时候,也可以使用此方法获得蛋白的一级序列信息,这个也就是蛋白的从头测序(De Novo)。由于质谱法简便快捷通量高,已成为首选的全长测序方法。

图2
二、百泰派克生物科技蛋白序列分析项目
1、项目文章一(N端测序)
标题:Phage defence system CBASS is regulated by a prokaryotic E2 enzyme that imitates the ubiquitin pathway
噬菌体防御系统CBASS由一种模拟泛素途径的原核E2酶调节
期刊:Nature microbiology
IF:20.5
时间:2024
研究概要:
基于环寡核苷酸的抗噬菌体信号系统(CBASS)是一种先天性原核免疫系统。CBASS由环GMP-AMP合成酶(cGAS)和CBASS相关蛋白组成,利用环寡核苷酸激活抗病毒免疫。一类主要的CBASS含有真核泛素结合酶的同源物,它要么是E1-E2的融合,要么是单一的E2。然而,单个E2在CBASS中的功能尚不明确。通过生化、遗传、低温电镜和质谱分析,发现粘质沙雷氏菌的E2酶通过模仿泛素化级联来调节cGAS。这包括cGAS C末端的加工,cGAS与半胱氨酸残基的偶联,cGAS与赖氨酸残基的连接,异肽键的裂解和多cGASylation。多cGASylation激活cGAS产生cGAMP, cGAMP作为抗病毒信号并导致细胞死亡。因此,研究结果揭示了E2在CBASS中的独特调节作用。
其中基于Edman降解法的N端测定由百泰派克提供。
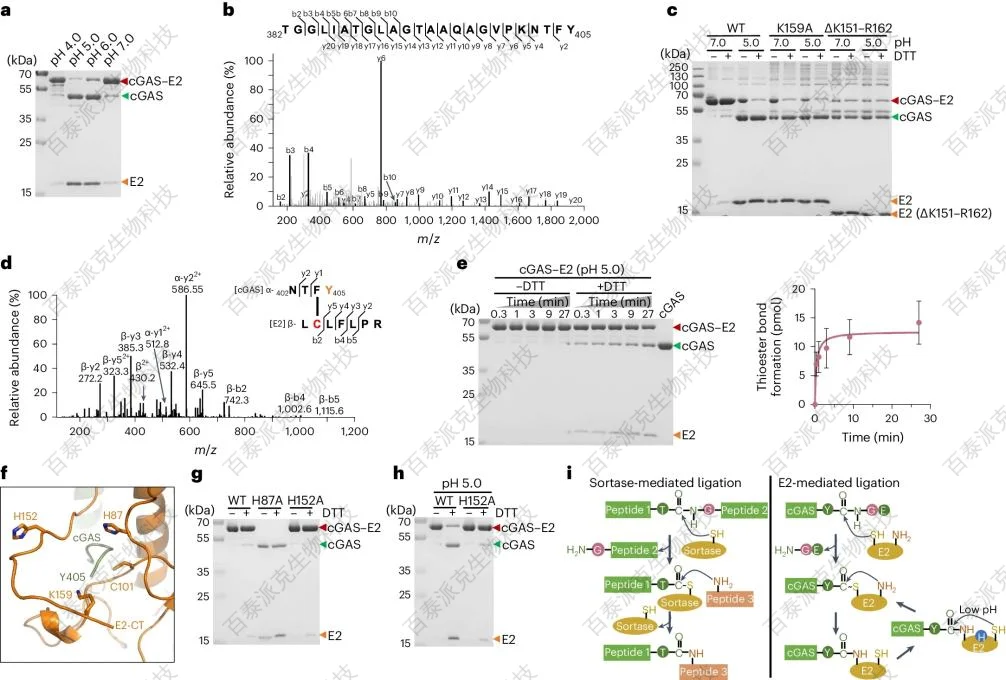
图3
2、项目文章二(N/C端测序)
标题:Bioengineered Human Serum Albumin Fusion Protein as Target/Enzyme/pH Three-Stage Propulsive Drug Vehicle for Tumor Therapy
生物工程人血清白蛋白融合蛋白作为肿瘤治疗的靶标/酶/pH三期推进药物载体
期刊:ACS Nano
IF:15.8
时间:2020
研究概要:
人血清白蛋白(HSA)具有生物相容性和长循环的特点,被广泛用作不溶性抗癌药物的载体,但也存在肿瘤靶向性弱、药物释放不可控等缺点。本研究通过基因融合技术,在HSA分离端引入多组氨酸(pHis)、基质金属蛋白酶-2 (MMP-2)酶切和Arg-Gly-Asp (RGD)肽,以提高HSA的生物学性能。毕赤酵母表达的蛋白可以自组装成3RGD-HSA-MMP-18His纳米颗粒(RHMH18 NPs),并将疏水药物紫杉醇(PTX)装载到多组氨酸胶束核心中。RHMH18 NPs由于rgd介导的ανβ3-整合素在肿瘤血管内皮上的特异性结合上调,导致肿瘤部位的治疗物质富集,从而表现出高效的肿瘤靶向活性。一旦到达肿瘤微环境,RHMH18 NPs被MMP-2切断,除去HSA-3RGD部分,留下小而带正电的组氨酸胶团,可以更有效地穿透肿瘤组织的深部。最后,组氨酸胶团成功地从溶酶体中逃脱,并根据pH释放药物。体内实验结果表明,三段式推进RHMH18 NPs具有良好的肿瘤抑制活性,副作用最小,为肿瘤治疗提供了基于蛋白质的药物传递系统的潜在策略。
为确认融合蛋白,采用Western Blot法测定其具体成分,基于质谱法的蛋白的N端和C端序列由百泰派克公司测定。
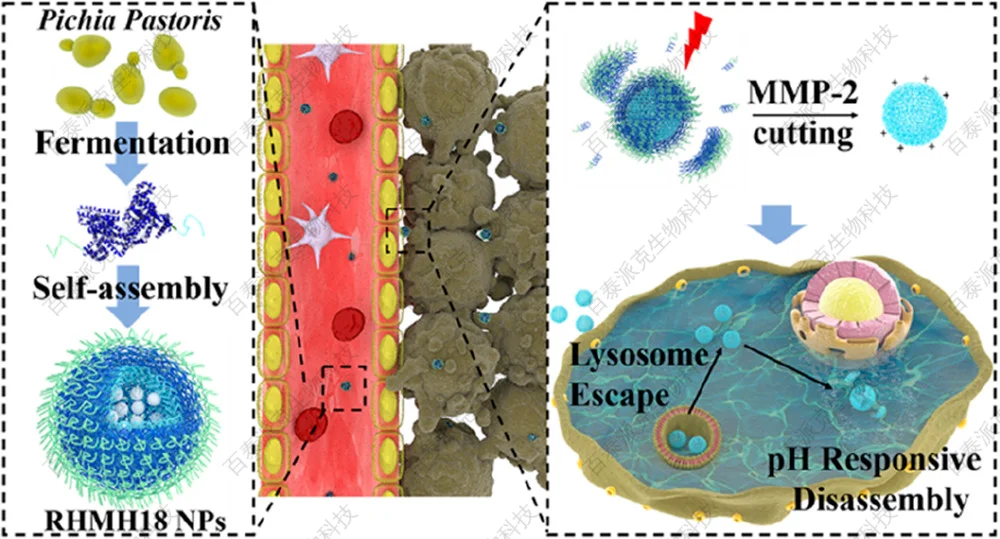
图4
3、项目文章三(蛋白De Novo测序)
标题:New fungal protein from Pleurotus ferulae lanzi induces AMPK-mediated autophagy and G1-phase cell cycle arrest in A549 lung cancer cells
新发现的阿韦兰侧耳真菌蛋白诱导A549肺癌细胞ampk介导的自噬和g1期细胞周期阻滞
期刊:International Journal of Biological Macromolecules
IF:7.7
时间:2023
研究概要:
从药用菌阿魏蓝菇中分离到一种具有抗非小细胞肺癌(NSCLC)活性的新蛋白PFAP。纯化方法包括在HiTrap辛基FF柱上进行疏水相互作用层析,在Superdex 75柱上进行凝胶过滤。凝胶电泳(SDS-PAGE)显示一条分子量为14.68 kDa的单条带。通过从头测序和液相色谱-串联质谱分析,PFAP被鉴定为由135个氨基酸残基组成的蛋白质,理论分子量为14.81 kDa。基于串联质量标签(TMT)的定量蛋白质组学分析和western blotting显示,在PFAP治疗后,AMP活化的蛋白激酶(AMPK)在NSCLC A549细胞中显著上调。下游调控因子哺乳动物靶雷帕霉素(mTOR)被抑制,导致自噬激活,P62、LC3 II/I等相关蛋白表达上调。PFAP通过上调P53和P21在细胞周期的G1期阻断NSCLC A549细胞,随后下调周期蛋白依赖性激酶的表达。在体内异种移植小鼠模型中,PFAP通过相同的机制抑制肿瘤生长。这些结果表明PFAP是一种具有抗NSCLC特性的多功能蛋白。
为得到新蛋白PFAP的序列,采用基于质谱的De Novo方法测定,此部分检测由百泰派克提供。
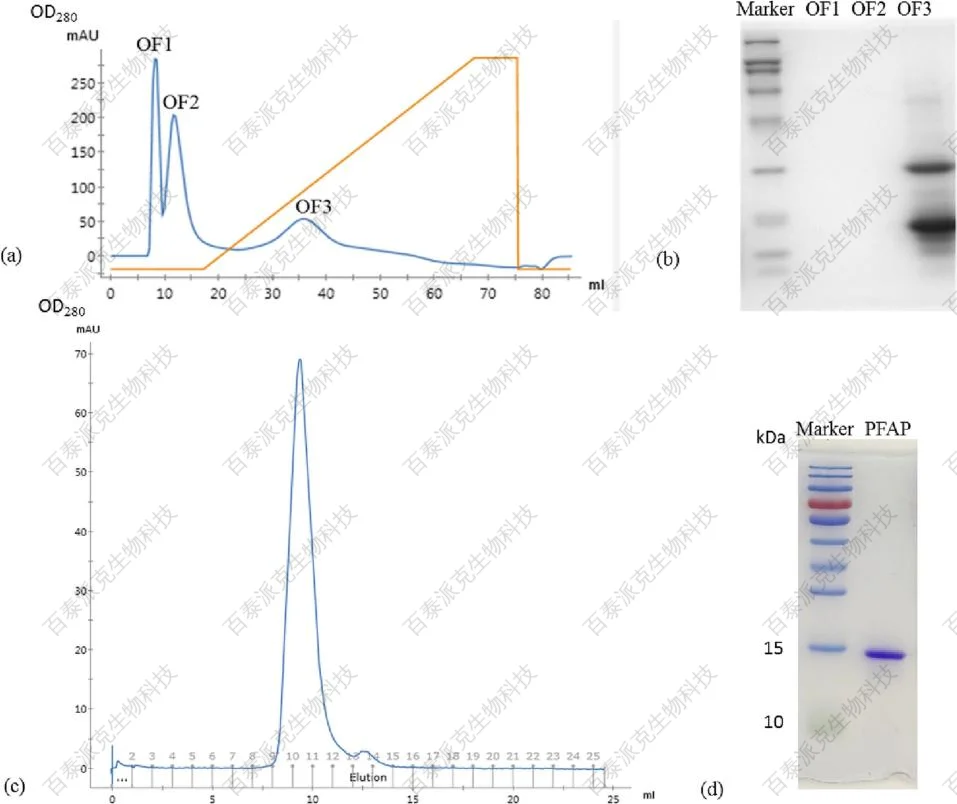
图5
百泰派克生物科技凭借丰富的蛋白质组学研究经验和强大的技术平台,致力于为科研机构、制药企业和生物技术公司提供高效、精准的蛋白序列分析检测服务。我们的团队由经验丰富的专业技术人员组成,能够根据不同的研究需求,量身定制最合适的分析策略,确保每一个项目都能够获得可靠的数据支持。无论是基础研究、药物开发还是临床诊断,百泰派克都能够为您提供全面的技术支持与解决方案,助力您的科研成果转化为实际应用。选择百泰派克,就是选择专业、高效与可靠的蛋白序列的分析检测合作伙伴。
参考文献:
1、Yan, Y., Xiao, J., Huang, F. et al. Phage defence system CBASS is regulated by a prokaryotic E2 enzyme that imitates the ubiquitin pathway. Nat Microbiol 9, 1566–1578 (2024).
2、Wang M, Zhang L, Cai Y, Yang Y, Qiu L, Shen Y, Jin J, Zhou J, Chen J. Bioengineered Human Serum Albumin Fusion Protein as Target/Enzyme/pH Three-Stage Propulsive Drug Vehicle for Tumor Therapy. ACS Nano. 2020 Dec 22;14(12):17405-17418.
3、Liu MH, Liu F, Ng TB, Liu ZK. New fungal protein from Pleurotus ferulae lanzi induces AMPK-mediated autophagy and G1-phase cell cycle arrest in A549 lung cancer cells. Int J Biol Macromol. 2023 Jul 31;244:125453.
相关服务
序列分析
关于我们
北京百泰派克生物科技有限公司致力于为生物/制药和医疗器械行业提供质量控制检测和项目验证等专业服务。公司实验室遵循NMPA、ICH、FDA和EMA等的法规和指导原则,通过CNAS/ISO9001双重质量体系认证,建立了完备的质量体系,数据冷热/异地备份,设备定期计量/期间核查,软件审计追踪,为客户提供一体化解决方案和技术服务,支持新药研发、药物申报注册和生产放行。
1.公司采用ISO9001质量控制体系,专业提供以质谱为基础的CRO检测分析服务;
2.获国家CNAS实验室认可,为客户提供符合全球药政法规的药物质量研究服务;
3.业务范围覆盖蛋白质组学、多肽组学、代谢组学、生物药物表征、单细胞分析、单细胞质谱流式、生信云分析以及多组学生物质谱整合分析等;
4.七大质量控制检测平台,满足您一站式服务需求;
5.服务3000+企业,10000+客户的选择;
6.致力于为您提供优质的生物质谱分析服务!
